QUAIS SÃO OS HORMÔNIOS DA FOME E DA SACIEDADE?
1. Insulina, o hormônio do “Armazenamento”:
A insulina é secretada pelo pâncreas para permitir que as células absorvam a glicose (açúcar no sangue) para produção de energia ou armazenamento em forme de açúcar no fígado ( glicogênio hepático) e açúcar na célula muscular ( glicogênio muscular).
Em geral, células saudáveis têm uma alta sensibilidade à insulina.
Mas quando as células são expostas constantemente a altos níveis de insulina, como resultado de uma ingestão constante de glicose (grande parte em razão de um consumo exagerado de alimentos processados, recheados de açúcares e farinhas refinadas que elevam os níveis de insulina acima do limite saudável), nossas células se adaptam reduzindo, na própria superfície, o número de receptores que reagem à insulina.
Em outras palavras, nossas células se dessensibilizam à insulina, gerando uma condição chamada “resistência à insulina”, que lhes permite ignorá-la e não absorver a glicose do sangue, o que pode culminar em maior estoque de gordura corpórea e consequentemente diabetes tipo 2.
- INSULINA ELEVADA FAVORECE ESTOQUE DE GORDURA E DESFAVORECE A QUEIMA!
- INSULINA ELEVADA FAVORECE: SÍNDROME METABÓLICA, OBESIDADE, SÍNDROME DOS OVÁRIO POLICÍSTICOS, CÂNCER E HIPERTENSÃO
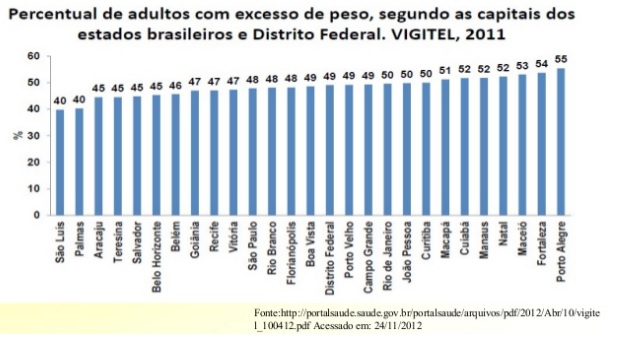
A esteatose hepática não alcoólica é um dos componentes da síndrome metabólica, foco de diversas agências de saúde mundiais nas duas últimas décadas.
No Brasil o índice de pessoas obesas ou com sobrepeso vem aumentando a cada ano.
O que fazer sobre isso?
Em um estudo realizado por pesquisadores das Universidades de Tokushima e Shizuoka no Japão, publicado no periódico American Journal of Physiology – Endocrinology and Metabolism em 2009, a esteatose hepática foi induzida em ratos, com uma dieta rica em sacarose (açúcar refinado).
Os ratos com esteatose hepática foram então colocados em duas dietas: uma dieta controle, rica em carboidratos, e outra pobre em carboidratos e rica em proteínas.
A dieta low carb com mais proteínas reverteu a esteatose nos roedores, ao contrário da dieta com mais carboidratos.
Deve-se reduzir a ingestão de carboidratos para reduzir a secreção crônica ou excessiva de insulina, reduzindo principalmente a ingestão de frutose, que é conhecida por causar resistência à insulina e hiperinsulinemia.
O consumo da frutose cresceu muito nos últimos 40 anos, devido ao seu uso generalizado em muitos alimentos e bebidas (doces, pudins, geleias, frutas enlatadas, bolos, refrescos em pó e principalmente refrigerantes).
Pesquisas recentes sobre o excesso de peso sugerem que o consumo de grandes quantidades de frutose pode estar relacionado ao desenvolvimento da síndrome metabólica.
Os estudos apontam o aumento do consumo de frutose associado ao sedentarismo com o aparecimento da esteatose hepática.
Além disto, a prática de exercícios físicos para queimar os depósitos de glicogênio e SENSIBILIZAR a insulina nos músculos esqueléticos são imprescindíveis.
“Deve-se reduzir a ingestão de carboidratos para reduzir a secreção crônica ou excessiva de insulina, reduzindo principalmente a ingestão de frutose, que é conhecida por causar resistência à insulina e hiperinsulinemia”
De acordo com trabalho publicado no periódico científico Arquivos Brasileiros de Endocrinologia & Metabologia, por pesquisadores brasileiros da Universidade Federal da Bahia, “o exercício físico:
- melhora a sensibilidade à insulina
- diminui a hiperinsulinemia
- aumenta a captação muscular de glicose
- melhora o perfil lipídico
- melhora hipertensão arterial
- eleva a sensação de bem-estar
- contribui para a perda de peso.
Um outro estudo prospectivo em 110.660 indivíduos seguidos por 6 anos mostrou que a prática diária de exercícios físicos diminuiu a incidência de diabetes mellitus em 46%.
2. Leptina, o hormônio da “Saciedade”:
À primeira vista, a leptina é um componente integral de um intrincado sistema fisiológico que regula o armazenamento, o equilíbrio e o uso de energia pelo organismo.
Além deste papel, a leptina sinaliza e modula o estado nutricional do organismo para outros sistemas fisiológicos.
A leptina é um hormônio produzido predominantemente pelo tecido adiposo branco em relação proporcional direta à massa corporal deste tecido, isto é, a massa total de tecido adiposo do organismo é o fator que mais está associado às concentrações de leptina no sangue.
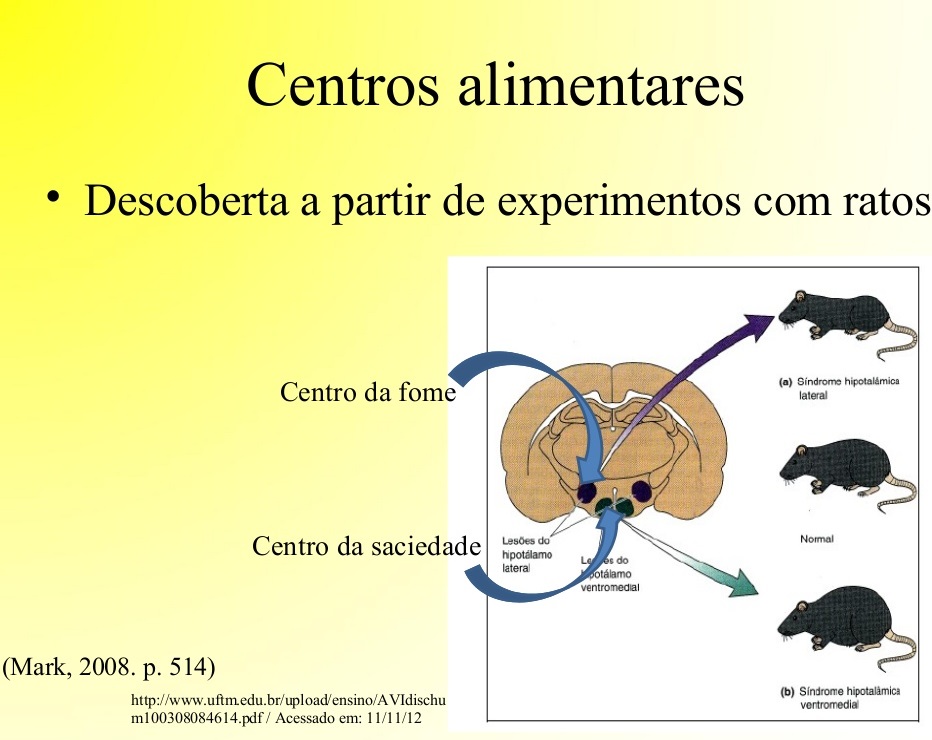
Este hormônio sinaliza ao centro da saciedade, no hipotálamo de que há bastante gordura armazenada e evita que se coma em excesso.
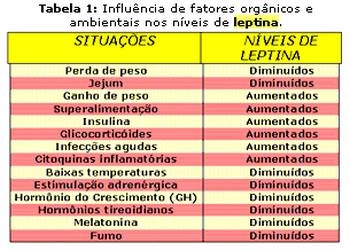
Porém, diversos mecanismos fisiológicos influenciam a síntese da leptina levando a oscilações nas quantidades de leptina intrinsecamente associadas com a massa de gordura.
O jejum, o exercício físico moderado e o frio causam uma queda nas concentrações plasmáticas da leptina e a alimentação após o jejum, glicocorticoides e insulina são fatores que estimulam a produção de leptina.
A maior parte das pessoas com obesidade têm níveis séricos de leptina proporcionais à sua massa de tecido adiposo, ou seja, a maioria das pessoas com obesidade não sofre de uma deficiência de leptina
. À semelhança do que se postula para o DM2, passou-se a considerar que a obesidade mais frequentemente encontrada na população é um estado onde há uma resistência aos efeitos de leptina.
Assim, postula-se que um acúmulo excessivo de leptina a curto prazo poderia levar a uma “down-regulation” dos receptores centrais e a um reajuste do seu efeito inibidor sobre o apetite.
Desta maneira, uma concentração acima do normal de leptina seria necessária para o mesmo efeito inibitório sobre o apetite. O que acontece quando a sinalização prejudicada não desencadeia no cérebro os estímulos para acalmar os hormônios da fome? O mau funcionamento está relacionado à obesidade, insulina cronicamente elevada e inflamação.
“A obesidade mais frequentemente encontrada na população é um estado onde há uma resistência aos efeitos de leptina, isto é o indivíduo tem mais dificuldade de ficar saciado”
O que fazer sobre isso?
- Evite alimentos inflamatórios, como óleos de sementes hidrogenadas como óleo de canola, milho , seja e girassol e foque nos ácidos graxos ômega-3.
- Certifique-se de que está dormindo bem, uma vez que a privação do sono está ligada a quedas nos níveis de leptina.
- O exercício físico, à semelhança da insulina também aumenta a sensibilidade à leptina aumentando o domínio sobre o apetite
- Outra forma de sensibilizar a insulina é praticar jejum intermitente e evitar comer de 3/3 horas desde que você não coma em demasia na refeição seguinte quando ficar mais de 3 horas sem se alimentar.
3. Grelina, o hormônio da “Fome”:
A grelina é liberada quando o estômago está vazio e cessa a liberação quando o estômago está distendido (cheio).
Ela estimula os neurônios orexígenos (NPY e AgRP) do centro da fome, no hipotálamo.
A concentração plasmática de grelina é mais alta antes de comer e mais baixa uma hora depois de comer.
Estudos demonstram que em certos pacientes obesos a grelina circulante não diminui, e por isso o cérebro não recebe o sinal para parar de comer.
Um grupo de pesquisadores norte-americanos e chineses publicaram em junho de 2017 no International Journal of Molecular Science, um trabalho que sugere que xarope de milho de alta frutose (HFCS) e a sacarose têm efeitos diferenciais sobre o metabolismo lipídico: enquanto a sacarose promove a obesogênese, o HFCS aumenta principalmente a inflamação e a resistência à insulina, sendo que a grelina confere efeitos protetores para essas disfunções metabólicas.
O que fazer sobre isso?
- Evite os carboidratos brancos, o açúcar e especialmente as bebidas açucaradas (refrigerantes) que não matam a fome e nem distendem o estômago.
- Coma proteínas em todas as refeição, especialmente no café da manhã, para promover a saciedade.
- Coma muita fibra, pois tem massa para distender fisicamente o estômago sem ganho calórico.
- Pratique exercícios físicos e não faça refeiçoes líquidas
Influência da atividade física no apetite
Um estudo realizado por pesquisadores espanhóis e publicado em junho de 2017 na Clinica e Investigacion en Arteriosclerosis, determinou a influência do exercício físico sobre o apetite, mudanças nas concentrações hormonais e mudanças em certas regiões neurais.
Para conseguirem isso, uma pesquisa bibliográfica foi realizada usando diferentes bases de dados. Os resultados mostraram que o exercício físico leva a alterações no apetite, na fome e na ingestão de energia.
Além disso, o exercício diminuiu os níveis de grelina, aumentou as concentrações de leptina e alterou a resposta de certas regiões neurais.
“O exercício físico diminui os níveis de grelina, aumenta as concentrações de leptina e altera a resposta de certas regiões neurais”
4. Peptídeo semelhante ao Glucagon 1 (GLP-1), o hormônio da “plenitude”:
O GLP-1 é produzido e liberado quando o alimento entra nos intestinos (íleo) para sinalizar ao nosso cérebro que estamos cheios. Já foi comprovado por cientistas que estudam o GLP-1 que ele afeta regiões no hipotálamo que controlam a saciedade em nosso organismo.
Sua principal ação, contudo, se dá nas células beta do pâncreas, que secretam a insulina. Por aumentar a quantidade de insulina no sangue, doses sintéticas desse hormônio são usadas para o tratamento de pessoas com diabetes tipo 2. A inflamação crônica reduz a produção de GLP-1, o que afeta negativamente a sinalização de saciedade (ficando sempre com fome).
O medicamento Liraglutida foi aprovado recentemente para tratamento de obesidade por conta deste mecanismo sacietógeno.
“Evite alimentos pró-inflamatórios e faça uma dieta anti-inflamatória”
O que fazer sobre isso.?
- Evite alimentos pro-inflamatórios (ricos em ácidos graxos ômega-6 como óleos vegetais de soja, algodão, milho e girassol, cereais refinados como pão francês, massas, bolachas de água e sal ou maisena, fubá e bolo simples, embutidos como salsicha, peito de peru e linguiça, tome probióticos, coma refeições ricas em proteínas, o que aumenta a produção de GLP-1.
- As refeições com vegetais de folhas verdes também aumentam os níveis de GLP-1.
- Os alimentos que controlam a inflamação são ricos em substâncias como alicina, ácidos graxos ômega-3 presentes em peixes como atum, sardinha e salmão, em frutas oleaginosas e em sementes como linhaça, chia e gergelim.
- São anti-inflamatórios também alimentos ricos em vitamina C como ervas aromáticas (alho, açafrão, curry e cebola) e frutas cítricas.
5. Colecistocinina (CCK), outro hormônio da “saciedade”:
A colecistocinina é produzida por células no trato gastrointestinal e sistema nervoso.
A CCK é liberada pelo duodeno sempre que comemos proteína ou gordura aumentando os sinais de saciedade enviados ao sistema nervoso, ao mesmo tempo que trabalha com o nosso estômago para tornar o processo de digestão mais lento, inibindo a motilidade e o esvaziamento gástrico.
O resultado disto é que nos sentimos mais cheios durante mais tempo!
A síndrome do intestino irritável (IBS) pode causar uma diminuição na produção de colecistocinina, fazendo você se sentir privado de energia.
O que fazer sobre isso?
- Estudos iniciais sugerem que a interação direta de colecistocinina e proteína dietética contribui para a resposta à saciedade.
- Gordura desencadeia a liberação de colecistocinina e a fibra alimentar pode dobrar a produção de colecistocinina. Para otimizar a libertação deste hormônio, coma proteínas e gorduras em cada refeição.
6. Peptídeo YY (PYY), o hormônio do “Controle”:
O PYY é um hormônio controlador do trato gastrintestinal que reduz o apetite.
Sua síntese ocorre nas glândulas endócrinas do intestino delgado e cólon.
Sua principal função é diminuir o apetite, aumentando a sensação de saciedade e diminuindo a motilidade intestinal.
A quantidade de hormônio secretada por essas células depende do tanto de calorias ingeridas, sendo estimuladas quando o alimento chega no intestino.
Os carboidratos simples refinados e os doces, são absorvidos antes que os intestinos liberem o hormônio PYY inibidor da fome.
O excesso de carboidratos / glicose então se transforma em gordura para ser armazenada mediante a excessiva produção de insulina
A resistência à insulina e o excesso crônico de açúcar no sangue, prejudicam a produção de PYY.
O PYY se comunica com os neurônios orexigênicos (estimuladores de apetite) e inibe o apetite através da inibição dos neurônios NPY estimuladores do apetite presentes no núcleo arqueado (ARC) do hipotálamo.
“Os carboidratos simples refinados, os doces e a frutose não oriunda de frutas sólidas são absorvidos antes que os intestinos liberem o hormônio PYY inibidor da fome”
A inibição do apetite induzida pelo estresse ocorre por esta mesma via. Assim, animais com a fome inibida pelo estresse, não respondem ao PYY exógeno, pois a via de inibição já está saturada. Recentemente foi demonstrado em humanos, o efeito de redução da ingestão de alimentos em voluntários obesos e com peso normal.
Em trabalho realizado por pesquisadores da UNICAMP, foram observados níveis reduzidos de PYY em obesos quando comparados aos controles magros. Isto sugere que a redução da produção de PYY pelo TGI possa estar relacionada à presença de obesidade em seres humanos.
O que fazer sobre isso?
- O açúcar ( glicose ) no sangue ( glicemia) em níveis saudáveis aumenta a resposta e a produção de PYY. As refeições à base de proteínas aumentam as concentrações de PYY, enquanto as fibras também aumentam a produção de PYY.
- Dietas gordurosas parecem estimular maior produção de PYY do que as ricas em carboidratos.
7. Neuropeptídeo Y (NPY), o hormônio “Estimulante”:
O NPY é um hormônio produzido no cérebro e sistema nervoso que “estimula” o apetite por carboidratos e é mais elevado durante os períodos de LONGOS jejuns ou privação alimentar. O estresse também induz a produção de NYP que leva à estimulação do apetite e ingesta excessiva de comida, conduzindo a um excesso de gordura em geral com maior ganho de gordura abdominal.
O que fazer sobre isso.
O jejum e a privação de alimentos podem estimular a liberação de NPY. Coma refeições completas regularmente com proteína muita e fibra prebiótica solúvel, faça jejum intermitente, com cautela, por pouco tempo. Estudos em animais demonstraram que jejuns muito longos, como os de mais de 24 horas, podem aumentar dramaticamente os níveis de NPY. A falta de proteína também aumenta a liberação do NPY. Comer pouca proteína tem demonstrado aumentar a liberação de NPY, o que leva à fome, aumento da ingestão de alimentos (principalmente carboidratos) e ganho de peso.
Referências
Consumo de frutose e exercício físico, impacto na síndrome metabólica
Doenças associadas à resistência à insulina/hiperinsulinemia, não incluídas na síndrome metabólica
CONSUMO DE FRUTOSE E IMPACTO NA SAÚDE HUMANA
Prevention and reversal of hepatic steatosis with a high-protein diet in mice.
Doenças associadas à resistência à insulina/hiperinsulinemia, não incluídas na síndrome metabólica
Tratamento do Diabetes Mellitus do Tipo 2: Novas Opções
O Controle Hipotalâmico da Fome e da Termogênese – Implicações no Desenvolvimento da Obesidade
Suppression of Ghrelin Exacerbates HFCS-Induced Adiposity and Insulin Resistance.
Review and analysis of physical exercise at hormonal and brain level, and its influence on appetite.





5 respostas
Caramba não tem jeito ter uma vida equilibrada com meditação e procurar estar de bem com a consigo mesmo, acredito que tem que ser o primordial para podermos bater de frente com todas as dificuldade que nosso organismo possa ter.
Ótimo artigo
Abraços
Obrigado
Dr. Roberto Franco, desde ja obrigado pelas informações. Doutor por quantas horas ou dias e saudável ficar em jejum, só ingerindo água mineral?
Existem inúmeros protocolos de jejum, o mais fácil é o de 16 h começando ao fim do jantar.
Eu simplesmente adorei essa explicação. Agora sim entendi tudo sobre hormônios. O Endocrinologista é a melhor solução. Estava a caminho do psiquiatra.